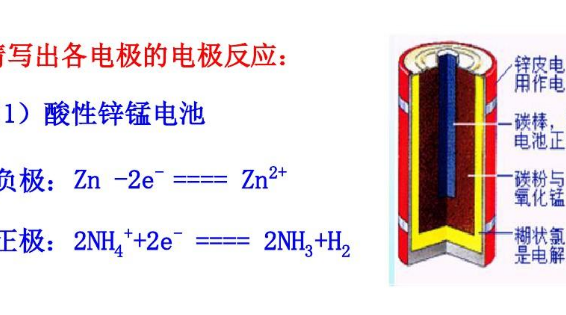
电极反应式是指在电化学装置中表示原子或离子在电极上得失电子发生氧化或还原反应的式子。
以铜锌原电池(稀硫酸为电解质溶液)为例,电极反应式。正极2H+ +2e-=H2↑。负极Zn-2e-=Zn2+。总反应式:Zn+2H+=Zn2++H2↑。
电极反应式的原则
电极反应式的书写原则电极反应基本上都是氧化还原反应,要遵循质量守恒、电子守恒及电荷守恒。除此之外还要遵循加和性原则:两电极反应式相加,消去电子后得电池总反应式。利用此原则,电池总反应式减去已知的一电极反应式得另一电极反应方程式。
共存性原则:碱性溶液中CO2不可能存在,也不会有H+参加反应或生成;同样酸性溶液,不会有OH参加反应或生成也不会有碳酸根离子的存在。根据此原则,物质得失电子后在不同的介质环境中所存在的形式不同。我们可以根据电解质溶液的酸碱性来书写。
同时还有1.根据电池装置图书写电极反应2.根据电池总反应书写电极反应3.二次电池电极反应的书写4.燃料电池电极反应的书写等。
标签:反应式,电极
版权声明:文章由 知识百问 整理收集,来源于互联网或者用户投稿,如有侵权,请联系我们,我们会立即处理。如转载请保留本文链接:https://www.zhshbaiwen.com/answer/6859.html